



《化学电源说课材料PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为851.5 KB,总共有21页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 21页
- 851.5 KB
- VIP模板
- ppt
- 数字产品不支持退货
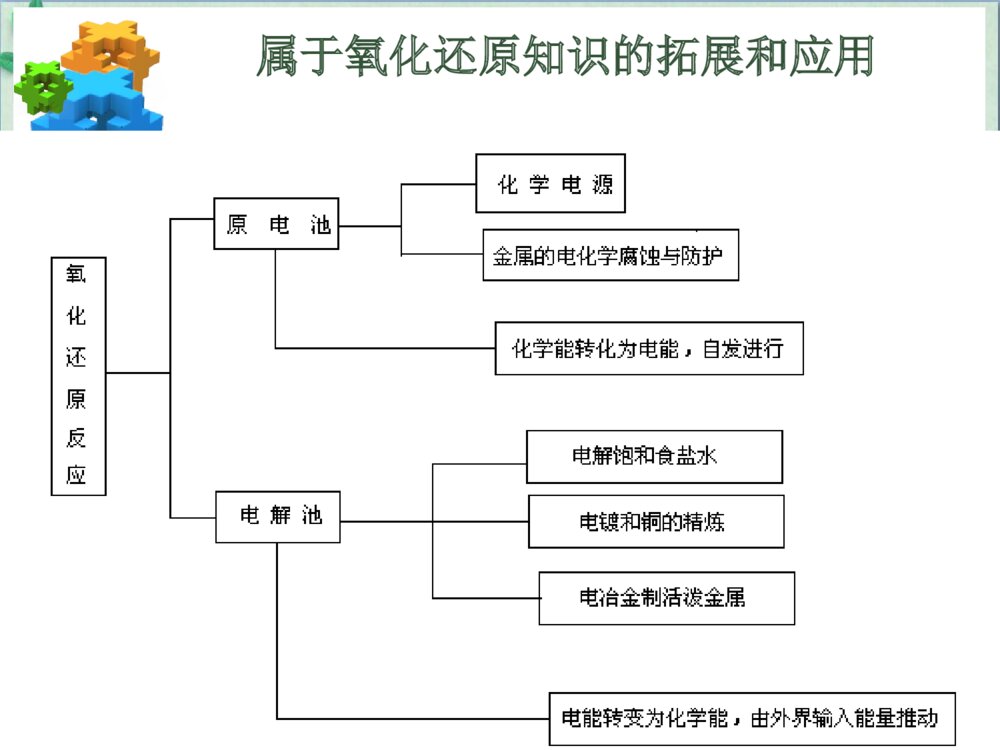
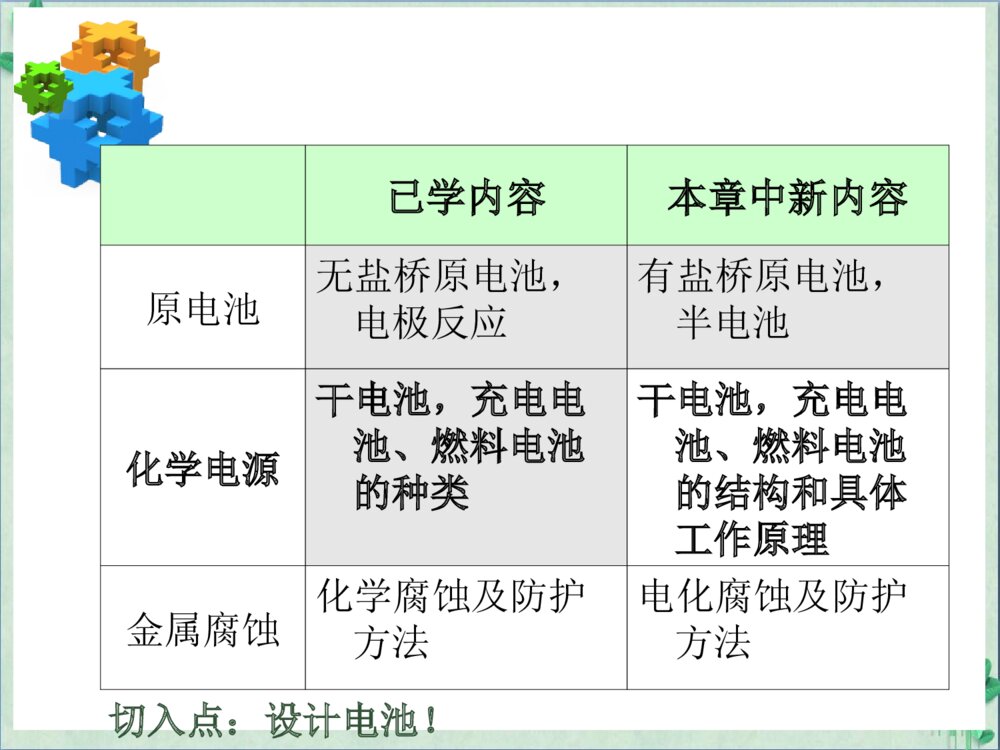
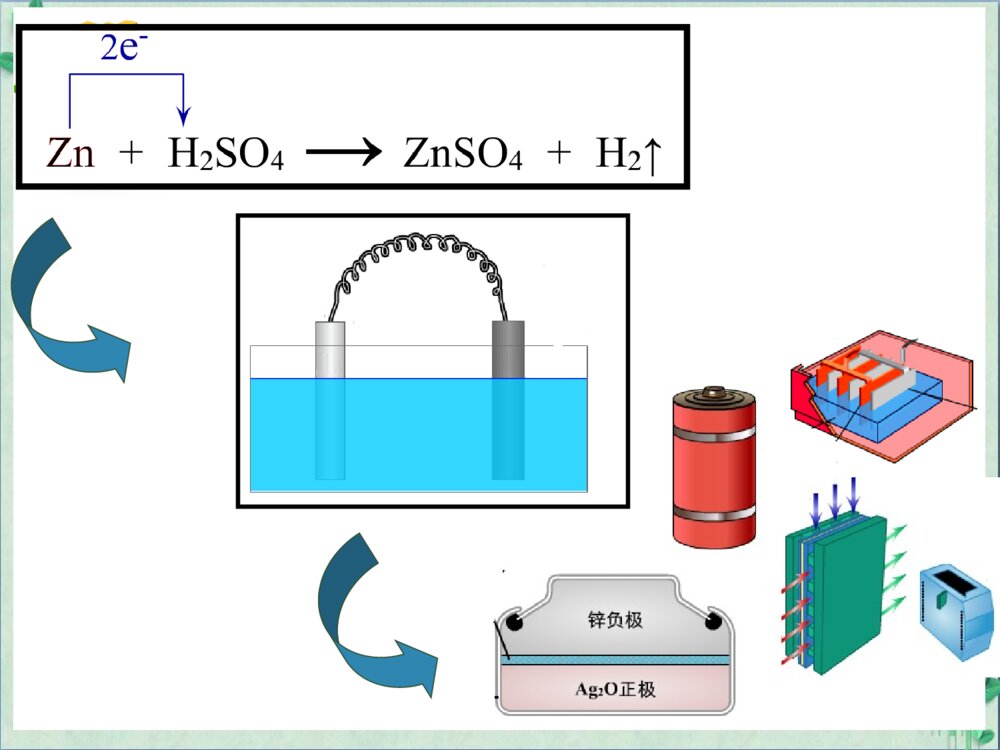
化学电源北京六十六中学说课材料Contents教材内容分析1教学目标设计2教学程序设计3教学反思4原电池的地位和作用知识功能分类属于能量的相互转化——研究化学反应与电能原电池知识内容来看原电池和电解属于氧化还原知识的拓展和应用.属于氧化还原知识的拓展和应用原电池原理的拓展应用和延伸通过化学电源加深对原电池的原理认识原电池化学电源化学电源的地位和作用课标要求分析现行高中大纲新课标原电池原理(以铜锌原电池为例)化学电源新型电池金属的电化学腐蚀与防护电解原理(以电解氯化铜为例)氯碱工业反应原理以氯碱工业为基础的化工生产简介铜的电解精炼镀铜3.举例说明化学能与电能的转化关系及其应用。4.认识研制新型电池的重要性。化学24.体验化学能与电能相互转化的探究过程,了解原电池和电解池的工作原理,能写出电极反应和电池反应方程式。5.通过查阅资料了解常见化学电源的种类及其工作原理,认识化学能与电能相互转化的实际意义及其重要应用。6.能解释金属发生电化学腐蚀的原因,认识金属腐蚀的危害,通过实验探究防止金属腐蚀的措施。选修4课标要求分析已学内容本章中新内容原电池无盐桥原电池,电极反应有盐桥原电池,半电池化学电源干电池,充电电池、燃料电池的种类干电池,充电电池、燃料电池的结构和具体工作原理金属腐蚀化学腐蚀及防护方法电化腐蚀及防护方法切入点:设计电池!教学目标设计1、基本教学目标:知识与技能(1)通过由氧化还原反应入手设计电池,深化学生对原电池的原理的认识。(2)通过电池的设计和新型电池的展示让学生了解新型电池的形成和工作原理。过程与方法在电池的设计过程中培养学生的知识迁移能力和发现问题、分析问题和解决问题的能力。情感态度价值观通过体验发明创造的过程,让学生产生创新的愉悦,增强为人类的文明进步学习化学的责任感和使命感。教学目标设计教学重点:(1)用原电池的基本原理分析和设计原电池,了解新型电池的结构和工作原理(2)体验理论设计到实际应用的创新过程。教学难点:体验理论设计到实际应用的创新过程。教学程序设计以Zn-Cu原电池为例,建立氧化还原反应和电池模型的联系练习通过氧化还原反应确定正负极,写出正负极反应并设计电池通过原电池模型向新型电池的转化动画,认识新型电池明线:学生活动设计说明为了解电池工作原理和电池结构做好知识和技能准备探索各新型电池的工作原理,巩固电极反应方程式的书写。为了解电池结构做好准备了解新型电池的结构暗线二:知识目标线化学符号向简单模型的转变巩固简单符号向模型转变的技能和方法了解简单模型向复杂模型的转变暗线一:能力方法线--构建学生最近发展区基本科学知识科学知识的简单应用科学知识的创新应用暗线三:科技应用主线暗线四:通过共性解决原理问题,通过个性解决创新问题设计说明四、教学反思1、多媒体的使用展示了符号向模型的转变、简单模型向复杂模型的转变,将思维的变化过程可视化,方便学生理解。2、尽力找寻学生的最近发展区,达到较好的学习效果。北京六十六中学ThankYou!ThankYou!说课材料属于能量的相互转化人教版山东科技版江苏教育版结构第一章、化学反应与能量的变化第四章电化学1、原电池2、化学电源3、电解池4、金属的电化学腐蚀第一章1、化学反应的热效应2、电能转化为化学能——电解3、化学能转化为电能——电池第一章1、化学反应的热效应2、化学与电能的转化3、金属的腐蚀与防护学生活动一:完成锌和硫酸反应的方程式,画出该锌铜原电池的装置图。:运用动画完成氧化还原反应与电池的相关性建构:设计意图:让学生了解设计电池的一般方法:在学生已有知识的基础上,建立符号与模型之间的联系,让学生巩固原电池的原理。学生活动二:利用下列氧化还原反应构建原电池二次电池(电解质为H2SO4)Pb+PbO2+2H2SO4序号氧化还原反应(总反应)负极正极装置图1Zn+Cu2+=Zn2++Cu2Fe+2Fe3+=3Fe2+3一次电池:(电解质是KOH)Zn+2H2O+2MnO2=2MnO(OH)+Zn(OH)24一次电池:名称为:锌锰干电池(电解质是NH4Cl)Zn+2NH4Cl+2MnO2=Mn2O3+ZnCl2+2NH3+H205锌银电池(电解质为KOH)Zn+Ag2O=ZnO+2Ag62PbSO4+2H2O7燃料电池——氢氧燃料电池(酸性电解质)2H2+O2=2H2O8燃料电池——甲烷燃料电池(KOH)CH4+2O2+2OH-=CO32-+3H2O9燃料电池——甲醇燃料电池(KOH)2CH3OH+3O2+4OH-=2CO32-+6H2O设计意图:让学生了解一些化学电源的工作原理,进一步练习和巩固原电池的原理;让学生能够熟练掌握设计电池的第一步骤。学生活动三:了解常见电池的结果和应用范围动画:电池的变脸(1)干电池(2)碱性电池(3)锌银电池(4)铅蓄电池(5)氢氧燃料电池关于氢氧燃料电池的批判性思考前面三个电池有何缺点?(1)需要很大的电能,干电池电能小。(2)寿命短,用几天就不行,宇宙飞船要连续用半年甚至一年。(3)工作不稳定返回



















